Sequenciação de mRNA: Sequência de mRNA, Fluxo de Trabalho Experimental e Aplicações
Introdução ao Sequenciamento de mRNA
Sequenciação de RNA mensageiro (mRNA-Seq) é uma técnica de alto rendimento importante utilizada para analisar a expressão génica em detalhe. Esta abordagem é amplamente utilizada na análise de padrões de expressão génica, variantes de transcritos e modificações de RNA. Ao sequenciar o mRNA celular, o mRNA-Seq fornece profundas percepções sobre as alterações na atividade génica sob várias condições fisiológicas e patológicas. Tais revelações são inestimáveis para os investigadores que visam decifrar os complexos mecanismos de regulação da expressão génica. O mRNA-Seq desempenha um papel importante em vários campos científicos, incluindo epigenética, oncologia, farmacologia e medicina personalizada.
O princípio fundamental do mRNA-Seq reside em aproveitar tecnologias de sequenciação de alto rendimento realizar uma avaliação quantitativa exaustiva de todos os genes dentro de um transcriptoma. Este método proporciona insights detalhados sobre os níveis de expressão génica, eventos de splicing alternativo, alterações estruturais transcriptómicas e a importância funcional dos RNAs não codificantes. Quando comparado com os métodos tradicionais de microarray, o mRNA-Seq exibe uma sensibilidade superior e gera uma tapeçaria de dados mais rica, capaz de revelar novos transcritos e formas de splicing alternativo. Assim, o mRNA-Seq é uma ferramenta indispensável para a exploração intricada da função génica e das redes regulatórias.
Fluxo de Trabalho Experimental:
O procedimento para mRNA-Seq abrange várias etapas essenciais:
1. Extração e Purificação de RNAO processo começa com a extração de RNA total de amostras celulares ou de tecido. Como o RNA ribossómico (rRNA) representa mais de 90% do conteúdo total de RNA, estratégias como a enriquecimento com esferas Oligo(dT) são rotineiramente aplicadas para isolar especificamente o mRNA, que é caracterizado por caudas de poliA. Aumentar a especificidade do mRNA neste ponto é crucial para melhorar a eficiência e a precisão do experimento.
2. Fragmentação de RNA e Transcrição ReversaO mRNA isolado é posteriormente fragmentado em pedaços menores, geralmente utilizando métodos químicos como aquecimento ou digestão enzimática. Após a fragmentação, a transcrição reversa é realizada com transcriptase reversa para converter os fragmentos de mRNA em DNA complementar (cDNA).
3. Construção de Biblioteca de cDNAO cDNA resultante é modificado através da adição de sequências de adaptadores específicas necessárias para a sequenciação. Dependendo do foco da investigação, pode ser utilizada a construção de bibliotecas específicas de cadeia, o que é particularmente importante para a análise de variantes de transcritos específicas.
 Esquema das Diferenças na Construção de Bibliotecas entre Sequenciação de mRNA Convencional e 3'-DGE. (Xiong, Y., et al.., 2017)
Esquema das Diferenças na Construção de Bibliotecas entre Sequenciação de mRNA Convencional e 3'-DGE. (Xiong, Y., et al.., 2017)
4. Sequenciação de Alto RendimentoA biblioteca de cDNA é então submetida a sequenciação de alto rendimento usando plataformas como Illumina, PacBio ou Oxford Nanopore, para capturar a informação de sequência dos fragmentos de mRNA.
5. Análise de DadosUma análise abrangente dos dados de sequenciação segue, envolvendo alinhamento, anotação e interpretação para obter informações sobre os níveis de expressão génica, variações de splicing e diversidade de transcritos. Esta análise é acompanhada por processos essenciais como controlo de qualidade, normalização de dados e análise de expressão diferencial.
Visão Geral Técnica
mRNA-Seq é uma tecnologia poderosa de alto rendimento com vantagens significativas, mas também alguns desafios. Manter a pureza e a integridade do RNA é crucial para evitar degradação ou contaminação que possam afetar os resultados. A utilização de amostras de RNA de alta qualidade é imperativa para obter dados de sequenciamento precisos. A fiabilidade dos dados depende da consideração cuidadosa de fatores como réplicas, configurações de grupos de controlo e seleção de amostras. Além disso, escolher a profundidade de sequenciamento apropriada é crítico; uma profundidade inadequada pode deixar de detetar transcritos de baixa abundância, enquanto uma profundidade excessiva pode levar a custos desnecessários. A normalização dos dados é vital para comparações entre diferentes amostras, ajudando a corrigir os preconceitos resultantes de variações na profundidade de sequenciamento.
Em conclusão, o mRNA-Seq fornece informações valiosas sobre a expressão génica. No entanto, alcançar resultados fiáveis requer um planeamento cuidadoso e a otimização tanto dos métodos experimentais como da análise de dados.
Serviços que pode estar interessado em
Quer saber mais sobre os detalhes do sequenciamento de mRNA? Confira estes artigos.:
Qual é a sequência de mRNA
O mRNA é uma molécula de RNA de cadeia simples transcrita a partir do DNA, transportando informação genética do DNA para os ribossomas, onde ocorre a síntese de proteínas no citoplasma. Esta sequência codifica as instruções para a produção de proteínas, e a sua estrutura é crucial para a estabilidade e eficiência da tradução da expressão génica em proteínas correspondentes.
Estrutura Detalhada do mRNA Eucariótico
1. Estrutura do Cap 5'
- Nas células eucarióticas, o mRNA possui um cap 5' contendo 7-metilguanosina (m7G). Este cap protege o mRNA da degradação por exonucleases e ajuda na ligação dos ribossomas para iniciar a tradução. Além disso, a estrutura do cap participa na regulação da expressão génica e facilita o transporte do mRNA do núcleo para o citoplasma.
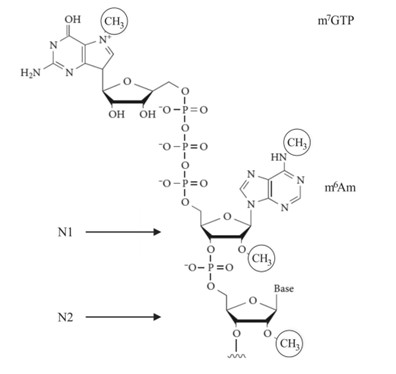 Estrutura do cap do mRNA eucariótico. (Jia, Longfei, et al., 2021)
Estrutura do cap do mRNA eucariótico. (Jia, Longfei, et al., 2021)
1. Região Não Traduzida 5' (5' UTR):
- A UTR 5' está localizada na extremidade 5' do mRNA, abrangendo desde o local de início da transcrição até logo antes do códon de início. Desempenha um papel fundamental na iniciação da tradução, ajudando a subunidade ribossómica pequena a escanear o mRNA para localizar o códon de início.
2. Quadro de Leitura Abertos (ORF):
- Esta é a região codificadora do mRNA, abrangendo a sequência entre o códon de início (AUG) e o códon de paragem, que é traduzida em proteína.
3' Região Não Traduzida (3' UTR):
- Encontrado a jusante do ORF, entre o códon de paragem e a cauda poli-A. O 3' UTR contém sequências reguladoras que governam a estabilidade do mRNA, a localização e a eficiência da tradução. Inclui a sequência de sinal de poliadenilação (AAUAAA), essencial para a adição da cauda poli-A.
4. Cauda Poly-A:
- A cauda poli-A é uma sequência de nucleotídeos de adenina adicionada à extremidade 3' do mRNA, tipicamente composta por 80 a 250 resíduos. A cauda ajuda a estabilizar o mRNA, protege-o da degradação e regula a iniciação da tradução. As proteínas ligadoras de poli-A (PABP) ligam-se à cauda poli-A, ajudando na proteção do mRNA.
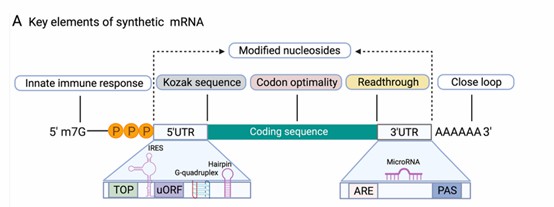 Representação esquemática de um mRNA sintético. (Jia, Longfei, et al., 2021)
Representação esquemática de um mRNA sintético. (Jia, Longfei, et al., 2021)
Papel e Diferenças entre o mRNA Procariótico e Eucariótico
O mRNA desempenha um papel central na expressão génica tanto em organismos procarióticos como eucarióticos, embora as modificações estruturais e pós-transcricionais diferem significativamente entre os dois.
Principais Diferenças entre mRNA Procariótico e Eucariótico:
| Recurso | mRNA procariótico | mRNA eucariótico |
|---|---|---|
| Estrutura do Cap 5' | Ausente | Presente (cap 7-metilguanosina, m7Gppp) |
| Cauda Poli-A | Ausente (pode ter caudas mais curtas sob certas condições) | Presente (tipicamente 80-250 resíduos de adenina) |
| Regiões Não Traduzidas (UTRs) | Curto, geralmente não envolvido na regulamentação. | Presente (inclui 5'UTR e 3'UTR, envolvido na regulação) |
| Intrões e Exões | Sem intrões (apenas exões) | Contém intrões (não codificantes) e exões (codificantes), necessitando de splicing. |
| Processamento Pós-transcricional | Processamento mínimo (sem emenda ou captação) | Modificações extensivas (capping, splicing e poliadenilação) |
| Estabilidade | Relativamente de curta duração (minutos a horas) | Mais estável, regulado pelo cap 5' e pela cauda poli-A 3' |
| Cronograma da Tradução | Pode iniciar imediatamente após a transcrição. | A tradução começa apenas após o processamento do mRNA e a exportação para o citoplasma. |
| Localização da Transcrição e Tradução | Ocorre no citoplasma (sem núcleo) | Transcrição no núcleo, tradução no citoplasma. |
| Interacção com Ribossomas | Liga diretamente os ribossomas pós-transcrição para tradução. | Requer exportação citoplasmática e interação do cap 5'-ribossoma para a tradução. |
Esta distinção sublinha os intrincados mecanismos regulatórios e as complexidades estruturais que diferenciam as funcionalidades do mRNA em procariotas e eucariotas, refletindo adaptações evolutivas no controlo da expressão génica.
O que a mRNA-Seq lhe diz
mRNA-Seq é uma técnica de alta capacidade transformadora, que decifra meticulosamente sequências de mRNA específicas de células para desvendar as complexidades da expressão génica e da transcriptómica. Esta metodologia oferece profundas percepções em várias dimensões críticas:
Quantificação da Expressão GénicaA mRNA-Seq facilita a medição precisa dos níveis de expressão génica numa vasta gama de amostras, permitindo assim a identificação de genes que são regulados de forma diferencial sob condições biológicas específicas. Uma aplicação valiosa inclui a comparação dos perfis de expressão de mRNA de células tumorais versus células normais para discernir genes implicados na oncogénese.
Variantes e Isoformas de TranscritosAlém de simplesmente quantificar a expressão génica, o mRNA-Seq é hábil em delinear várias variantes de transcritos produzidas através do splicing alternativo, cada uma potencialmente codificando isoformas proteicas funcionalmente distintas. Esta análise sublinha a importância da técnica na exploração da complexidade transcriptómica e da diversidade funcional.
Emendação e Dinâmicas Pós-TranscricionaisA tecnologia destaca-se na caracterização de padrões de splicing e modificações pós-transcricionais, como a metilação, que podem influenciar profundamente a expressão génica. A identificação de padrões de splicing aberrantes, frequentemente associados a distúrbios genéticos, exemplifica a utilidade do mRNA-Seq na elucidação de novos mecanismos de doença.
Identificação de Novos Genes e TranscritosA mRNA-Seq desempenha um papel fundamental na descoberta de genes previamente não anotados e novos transcritos, particularmente em espécies ou tipos celulares pouco explorados. Isso melhora a nossa compreensão genómica, oferecendo novas perspetivas sobre os papéis biológicos e as vias da doença.
Aplicações de mRNA-Seq
A adaptabilidade do mRNA-Seq encontra relevância em múltiplos campos de investigação:
Análise da Expressão Génica: Ao avaliar as alterações de expressão sob diversas condições, o mRNA-Seq informa sobre os mecanismos regulatórios dos genes. É particularmente eficaz na investigação de doenças, onde ajuda a identificar mudanças de expressão relevantes para patologias e a identificar potenciais alvos terapêuticos.
Genómica do Cancro: Dentro da oncologia, o mRNA-Seq é fundamental para destacar as diferenças na expressão génica entre tecidos malignos e normais. Esta abordagem ajuda a descobrir genes cruciais para o desenvolvimento e progressão do tumor e identifica biomarcadores e alvos terapêuticos chave.
Medicina de Precisão: mRNA-Seq sustenta os avanços na medicina personalizada, onde perfis de expressão de mRNA individuais apoiam o desenvolvimento de estratégias terapêuticas direcionadas—cruciais no tratamento do câncer para otimizar a seleção de medicamentos e os regimes terapêuticos.
Investigação sobre Splicing e Transcriptómica: A técnica é vital para investigar padrões de splicing, especialmente dada a associação de muitas doenças, particularmente as genéticas, com irregularidades de splicing. O mRNA-Seq fornece informações essenciais para inovações diagnósticas e terapêuticas precoces.
Em conclusão, o mRNA-Seq oferece uma visão abrangente da dinâmica da expressão génica, isoformas de transcritos, eventos de splicing e modificações pós-transcricionais. Isso torna-o uma ferramenta indispensável na investigação básica, no estudo dos mecanismos da doença, em estratégias terapêuticas personalizadas e no desenvolvimento de medicamentos. A utilização do mRNA-Seq enriquece a nossa compreensão das redes regulatórias génicas, estabelecendo uma base científica sólida para avanços no diagnóstico de doenças, tratamento e progresso farmacêutico.
Qual é a diferença entre RNA-Seq e mRNA-Seq?
Sequenciação de RNA (RNA-Seq) e mRNA-Seq são duas técnicas genómicas prevalentes utilizadas para analisar transcriptomas celulares, cada uma com áreas de foco distintas. O seguinte delineia as principais diferenças entre estas metodologias:
| Características | RNA-Seq Total (RNA-Seq) | mRNA-Seq |
|---|---|---|
| Sequenciamento de Alvo | Abrange todos os tipos de RNA (tanto codificantes como não codificantes), como mRNA, rRNA, tRNA, miRNA, etc. | Alvo principalmente o RNA codificante, especificamente o mRNA, frequentemente excluindo outros tipos de RNA. |
| Métodos de Preparação de Amostras | Envolve a depleção de rRNA seguida pela enriquecimento ou seleção de vários tipos de RNA. | Emprega técnicas de enriquecimento em poli(A) para isolar especificamente o mRNA, removendo eficazmente o rRNA. |
| Âmbito de Aplicação | Oferece dados de transcriptoma abrangentes, incluindo a análise de RNA codificante e não codificante. | Focado na análise da expressão génica, ideal para estudos de mRNA e suas variações de expressão. |
| Sensibilidade dos Dados de Sequenciação | Alta sensibilidade para RNA não codificante (como lncRNA e miRNA). | Mais focado em mRNA, proporcionando insights mais profundos sobre regiões codificadoras. |
| Requisito de Amostra | Exige quantidades de amostra maiores devido ao sequenciamento de todos os tipos de RNA, resultando em uma saída de dados substancial. | Exige quantidades de amostra menores e alcança uma maior profundidade de sequenciação devido ao enriquecimento de mRNA. |
| Custo | Custos mais elevados devido a requisitos extensivos de dados e recursos computacionais. | Custos mais baixos, uma vez que se limita ao sequenciamento de mRNA enriquecido, gerando menos dados. |
| Resultados Analíticos | Facilita a análise de todas as transcrições, tanto codificantes como não codificantes, adequadas para descobrir transcrições novas. | Analisa principalmente RNA codificante, inestimável para estudos de expressão génica, particularmente na investigação de doenças. |
| Cenários Apropriados | Adequado para compreender detalhes completos do transcriptoma, incluindo RNA não codificante e modificações pós-transcricionais. | Aborda principalmente a expressão génica e as variações de transcritos, sendo particularmente útil na investigação de biomarcadores. |
Comparação Detalhada:
Tipos de RNA Alvo:
- RNA-Seq Total: Envolve-se com uma miríade de moléculas de RNA dentro de uma amostra, ideal para investigações transcriptómicas de espectro completo.
- mRNA-Seq: Exclusivamente sintonizado com mRNA, otimizando para estudos sobre expressão génica e mecanismos regulatórios.
Métodos de Preparação e Enriquecimento de Amostras:
- RNA-Seq totalNormalmente começa com a remoção de rRNA, otimizando a alocação de recursos de sequenciação.
- mRNA-SeqAproveita a seleção de poli(A) para enriquecer o mRNA, garantindo uma maior profundidade de sequenciação com material mínimo.
Áreas de Pesquisa Aplicáveis:
- RNA-Seq TotalAdequado para uma exploração transcriptómica profunda, particularmente em torno de RNA não codificante, variantes de splicing e modificações.
- mRNA-SeqDestinado a analisar a expressão génica, quantificar transcritos e investigar mecanismos regulatórios e genes associados a doenças.
Custo e Volume de Dados:
- RNA-Seq TotalGera volumes de dados significativos, incorrendo em custos consideráveis—frequentemente necessitando de 100 a 200 milhões de leituras por amostra.
- mRNA-SeqMais economicamente viável com menor produção de dados, frequentemente exigindo 25–50 milhões de leituras por amostra, particularmente vantajoso com material inicial limitado.
Escolhendo entre mRNA-Seq e Total RNA-Seq:
A decisão de usar RNA-Seq total ou mRNA-Seq deve alinhar-se com os objetivos de pesquisa e as limitações experimentais:
- Optar por RNA-Seq Total para análises aprofundadas que abrangem todos os tipos de RNA, especialmente ao direcionar RNAs não codificantes ou caracterização transcriptómica extensa.
- Escolher mRNA-Seq para estudos centrados na expressão génica, particularmente análises focadas em mRNA, com considerações de limitações de amostra e orçamento.
Ambas as metodologias oferecem vantagens e limitações distintas, exigindo uma avaliação deliberada do tipo de amostra, objetivos de pesquisa, recursos financeiros e profundidade de análise desejada antes da execução.
Referências:
- Xiong, Y., Soumillon, M., Wu, J. et al.Uma Comparação entre Sequenciamento de mRNA com Bibliotecas Aleatoriamente Primadas e Direcionadas a 3'. Relatórios Científicos 7, 14626 (2017). https://doi.org/10.1038/s41598-017-14892-x
- Jia, Longfei, e Shu-Bing Qian. "Engenharia de mRNA terapêutico de ponta a ponta." Contas de Pesquisa Química 54.23 (2021): 4272-4282. https://doi.org/10.1021/acs.accounts.1c00541
- Gong, Haoran, et al. "Otimização integrada de sequências de mRNA usando aprendizagem profunda." Briefings em Bioinformática 24.1 (2023): bbad001. https://doi.org/10.1093/bib/bbad001
- Wang, Y., Zhang, Z., Luo, J. et al.Vacina de mRNA: uma estratégia terapêutica potencial. Câncer Mol 20, 33 (2021). https://doi.org/10.1186/s12943-021-01311-z
- Stark, R., Grzelak, M. & Hadfield, J. Sequenciação de RNA: os anos da adolescência. Nat Rev Genet 20, 631–656 (2019). https://doi.org/10.1038/s41576-019-0150-2


 Diretrizes para Submissão de Amostras
Diretrizes para Submissão de Amostras
