Melhores Práticas para Projetar um Experimento de Sequenciação Cut&Tag
CUT&Tag (que combina tecnologias de marcação e sequenciação) é um método de análise genómica altamente eficiente, amplamente utilizado no estudo de interações proteína-DNA, epigenética e muitas outras questões biológicas. Para garantir o sucesso dos experimentos CUT&Tag, é essencial seguir as melhores práticas ao desenhar os experimentos. Este artigo apresenta essas melhores práticas para ajudar os investigadores a obter resultados experimentais fiáveis e de alta qualidade.
I. Princípios Fundamentais e Planeamento Pré-Experimental do Design Experimental
Correspondência entre Tipo de Alvo e Design Experimental
- Modificações de Histonas (por exemplo, H3K27me3, H3K4me3): Devem ser selecionados anticorpos de alta especificidade para ChIP, e a sua aplicabilidade na espécie alvo deve ser validada. Por exemplo, o anticorpo H3K27me3 da CST (Cell Signaling Technology) (número de catálogo #9733) demonstrou eficácia em vários estudos.
- Fatores de Transcrição (por exemplo, CTCF, STAT3): Devem ser preferidos anticorpos com anticorpos secundários pré-adsorvidos para reduzir a reatividade cruzada, e a especificidade do anticorpo deve ser validada através de experiências de knockout/knockdown.
- Estudos de célula única: A viabilidade celular (viabilidade >85%) e a integridade nuclear (membrana nuclear intacta sem ruptura ao microscópio) devem ser avaliadas, e a contagem inicial de células deve ser controlada entre 1.000 e 10.000 células.
Procedimento Padrão de Preparação de Amostras
- Coleta e Lavagem de Células:
- Células em Suspensão: Coletar diretamente por centrifugação (300×g, 5 min) e lavar duas vezes com PBS.
- Células aderentes: Após a digestão com tripsina, ressuspender em PBS pré-arrefecido para evitar danos mecânicos que possam levar ao vazamento de DNA.
- Fixação e permeabilização:
- Experimentos de modificação de histonas: Não é necessário o entrelaçamento. Permeabilize diretamente com Digitonina (1,5–3 μg/mL) durante 10 minutos para manter o estado nativo da cromatina.
- Experimentos com fatores de transcrição: Não é necessário cruzamento. Tal como nos estudos de modificação de histonas, a permeabilização deve ser realizada diretamente com Digitonina. Isto preserva o estado nativo da cromatina, garante a eficiência ótima das reações in situ tanto para os anticorpos como para a enzima Tn5, e assim produz dados com uma elevada relação sinal-ruído.
- Extração nuclear:
- Lisar membranas celulares utilizando um tampão hipotónico (10 mM Tris-HCl, 10 mM NaCl) para preservar núcleos intactos.
- Confirmar a viabilidade nuclear >90% através da coloração com azul de trypan e observar a uniformidade da morfologia nuclear ao microscópio.
Para um guia introdutório mais detalhado sobre sequenciação CUT&Tag, consulte "O que é a Sequenciação Cut&Tag? Um Guia Completo para Iniciantes".
 Otimização experimental do CUT&Tag (Abbasova L et al., 2025)
Otimização experimental do CUT&Tag (Abbasova L et al., 2025)
Diretrizes para o Manuseio de Tipos de Amostras Especiais
Amostras de Tecidos (Células Não Cultivadas)
- Amostragem e Preservação: O tecido fresco deve ser imediatamente congelado rapidamente em azoto líquido (armazenar a -80°C por ≤3 meses), ou incorporado em OCT e depois congelado a -80°C (evitar ciclos repetidos de congelamento e descongelamento).
- Procedimento de Dissociação: Digeste com colagenase IV (1 mg/mL) + DNase I (10 U/mL) a 37°C durante 30 minutos, depois filtre através de uma malha de 70 μm para obter uma suspensão de células únicas.
Amostras FFPE (Tecido Clínico Incorporado em Parafina)
- Desparafinação e Recuperação: Desparafinação duas vezes com xileno (10 minutos cada vez) → Hidratação em etanol em gradiente → Recuperação de antígenos a 95°C durante 20 minutos com tampão de citrato de sódio (pH 6.0).
- Notas-chave: O DNA de amostras FFPE é propenso à fragmentação; encurte o tempo da reação de transposição para 3–5 minutos e evite fragmentos que sejam demasiado pequenos (<100 bp).
Amostras Raras (por exemplo, células tumorais circulantes, CTCs)
- Volume Inicial: Mínimo de 500 células. As células vivas devem ser enriquecidas usando esferas magnéticas ConA (com concanavalina A) para evitar a contaminação por DNA de células mortas.
- Medidas de Prevenção de Perdas: Utilize tubos de centrifugação de baixa adsorção durante todo o processo. Após a incubação com esferas magnéticas, ressuspenda suavemente as células em PBS (≤5 vezes).
II. Operação Refinada dos Principais Passos Experimentais
Incubação de Anticorpos e Captura de Sinal
- Incubação com Anticorpo Primário:
- Relação de diluição do anticorpo de histona: 1:100–1:200 (por exemplo, CST #9733).
- Relação de diluição do anticorpo do fator de transcrição: 1:50–1:100 (por exemplo, Abcam #ab150471).
- Condições de incubação: Incubar durante a noite (12–16 horas) a 4°C com rotação ou à temperatura ambiente (25°C) durante 2 horas para garantir uma ligação adequada do anticorpo ao local-alvo.
- Ponte de Anticorpo Secundário:
- Utilize um anticorpo secundário de fusão Proteína A/G (por exemplo, Jackson ImmunoResearch #115-005-003) e incube à temperatura ambiente durante 1 hora para melhorar a direcionamento do complexo Tn5.
- Utilize um tampão de lavagem especializado, pré-arrefecido, contendo Digitonina para manter o estado permeabilizado dos núcleos e remover eficazmente anticorpos ligados de forma não específica.
Controlo Preciso da Tagmentação
- Preparação de Complexo Enzimático:
- Recomenda-se o uso de uma enzima de fusão pA-Tn5 pré-calibrada (como a Biotech Cat#TD902), com uma unidade de atividade ≥50 U/μL.
- Sistema de Reação: 1× Tampão de Tagmentação (contendo 10 mM MgCl₂), evitando a introdução de componentes inibitórios como SDS.
- Otimização das Condições de Ativação:
- Temperatura: Incubar a 37°C durante 5–10 minutos. Uma incubação excessiva levará a uma clivagem excessiva de DNA (fragmentos <50 bp).
- Terminação: Adicione EDTA (20 mM) ou proteinase K (digeste a 55°C durante 30 minutos) para inativar a atividade da enzima Tn5.
Padronização da Construção de Bibliotecas e Controlo de Qualidade
- Extração de DNA:
- Utilize a purificação com esferas magnéticas (como as esferas AMPure XP) para remover transposases e proteínas não ligadas.
- Seleção do Tamanho de Fragmentos de DNA: Fragmentos de 100–600 bp foram recuperados em gel utilizando o sistema BluePippin, garantindo uma percentagem de biblioteca eficaz >80%.
- Otimização da Amplificação por PCR:
- Seleção de Enzimas de Alta Fidelidade: KAPA HiFi HotStart ReadyMix (taxa de erro <0,02%).
- Controlo do Número de Ciclos: 10–12 ciclos (aumentar para 15 ciclos para quantidades iniciais baixas) para evitar sobre-amplificação e viés.
- Normas de Controlo de Qualidade:
- Análise de Fragmentos: O Bioanalisador Agilent 2100 mostrou um pico principal entre 200–300 bp sem caudas significativas.
- Qualidade de Sequenciamento: Plataforma Illumina NovaSeq, pontuação média de qualidade Phred Q30 >90%, conteúdo de GC 40–60%.
III. Integração Multi-ômica e Design Experimental de Alto Rendimento
Estratégias de Otimização para Processamento Paralelo de Múltiplas Amostras
- Aplicação da Plataforma de Automação:
- Utilize placas de 96 poços combinadas com um sistema de separação por beads magnéticos (como o Beckman Coulter Biomek i7) para automatizar todo o processo de incubação de anticorpos, lavagem e reações de transposição, reduzindo o erro humano.
- Volume de reação recomendado: 50 μL/amostra, garantindo homogeneidade dos reagentes em volumes iniciais baixos.
- Princípios de Design de Códigos de Barras:
- Estratégia de indexação de dupla extremidade: combinação de índices i5/i7 (como Illumina Nextera XT), distância de Hamming ≥3, evitando saltos de índice.
- Adição de amostra de controlo interno: Configurar controlo de IgG e controlo de entrada para cada lote para avaliação de ruído de fundo e calibração de picos.
Análise Conjunta de Dados Multi-ómicos
- Integração ATAC-seq:
- Utilize a sobreposição entre os dados de H3K4me3 do CUT&Tag e as regiões abertas no ATAC-seq para identificar promotores/enhancers ativos.
- Ferramentas recomendadas: HOMER (annotatePeaks.pl) para anotação funcional e base de dados Cistrome DB para alinhamento com elementos regulatórios conhecidos.
- análise de associação de RNA-seq:
- A triagem diferencial de genes (DESeq2, padj<0,05) e a análise de interseção de picos CUT&Tag foram utilizadas para construir uma rede de interação de elementos regulatórios de genes.
- Ferramentas de visualização: UCSC Genome Browser ou IGV para exibir resultados de co-localização.
IV. Problemas Comuns e Soluções Aprofundadas
| Problema | Análise de Causas | Solução | Caso de Referência |
|---|---|---|---|
| FRiP < 5% | Baixa eficiência de ligação de anticorpos ou atividade insuficiente da transposase. | Verificar a especificidade dos anticorpos (usando linhas celulares knockout), otimizar o tempo de reação de transposição. | Caso BioTechPack: FRiP aumentou para 18% após a otimização do anticorpo H3K27me3 |
| Enriquecimento de TSS Insuficiente | Lise nuclear incompleta ou permeabilização excessiva | Ajuste o tempo de permeabilização (5–10 minutos), use NP-40 em baixa concentração. | Solução iGeneBio: Permeabilização com digitonina + Captura com esferas magnéticas de ConA |
| Viés de Amplificação de Biblioteca | Número de ciclos de PCR inadequado ou qualidade do DNA molde deficiente | Otimizar o número de ciclos (10–12 ciclos), purificar o ADN para uma concentração >5 ng/μL | Kit Novozyme TD901: Q30 > 95% após amplificação de 12 ciclos |
| Efeitos de Lote Significativos | Flutuações nas condições experimentais ou desordem na sequência de processamento da amostra | Utilize uma plataforma automatizada, incluindo amostras de controlo dentro do mesmo lote. | Processo BioTechPack: placa de 96 poços + separação por esferas magnéticas, CV em lote < 5% |
V. Fluxo de Trabalho de Análise de Dados Detalhada
Processamento de Dados Brutos
- Controlo de Qualidade e Filtragem: O FastQC deteta bases de baixa qualidade (qualidade Phred <20) e contaminação por adaptadores, e faz o corte utilizando o Trimmomatic (parâmetros: ILLUMINACLIP:TruSeq3-SE:2:30:10 LEADING:3 TRAILING:3 SLIDINGWINDOW:4:15 MINLEN:36).
- Refinamento de dados: O ficheiro BAM foi ordenado e indexado utilizando o samtools para gerar o ficheiro final para a análise subsequente. Nota: Na análise de dados CUT&Tag, o passo de marcação de duplicados de PCR com base em coordenadas (por exemplo, utilizando o Picard MarkDuplicates) deve ser ignorado.
Identificação e Anotação de Picos
- Chamada de Picos MACS2:
- Para picos 'estreitos' (por exemplo, fatores de transcrição, H3K4me3): Use macs2 callpeak -t treatment.bam -c IgG_control.bam -f BAMPE -g hs -q 0.05. Se estiver a trabalhar com dados de ponta única ou quando for necessária uma correção explícita para o deslocamento do Tn5, podem ser utilizados os parâmetros --nomodel --shift -75 --extsize 150.
- Para picos 'amplos' (por exemplo, H3K27me3, H3K9me3): O parâmetro --broad deve ser adicionado, juntamente com um limiar mais relaxado, por exemplo: macs2 callpeak -t treatment.bam -c IgG_control.bam -f BAM -g hs --broad --broad-cutoff 0.1.
- Anotação Funcional: O pacote `ChIPseeker` anota regiões genómicas (promotores, exões, potenciadores) e correlaciona-as com dados de expressão génica (por exemplo, a base de dados GEO).
- Análise e Visualização Avançadas:
- Enriquecimento de Motivos: HOMER (findMotifs.pl) ou MEME Suite identifica sequências centrais de locais de ligação (por exemplo, o motivo conservado de CTCF: CCTCCTC).
- Análise Diferencial: O DESeq2 filtra picos expressos diferencialmente (padj < 0,05) e o `clusterProfiler` realiza a análise de enriquecimento GO/KEGG.
- Ferramentas de Visualização: O IGV gera faixas de cobertura e mapas de calor para mostrar a distribuição genómica dos locais de ligação da proteína alvo.
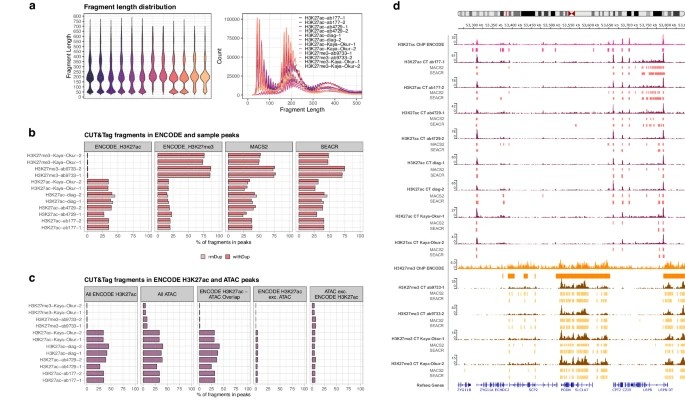 Métricas de controlo de qualidade para dados CUT&Tag (Abbasova L et al., 2025)
Métricas de controlo de qualidade para dados CUT&Tag (Abbasova L et al., 2025)
VI. Comparação das Vantagens e Limitações Técnicas
| Vantagens | Limitações | Contramedidas |
|---|---|---|
| Requisito de amostra extremamente baixo (nível de célula única) | Fortemente dependente da qualidade e especificidade dos anticorpos. Para alvos com abundância extremamente baixa, pode ser necessário otimizar as condições experimentais (por exemplo, aumentando o número inicial de células, prolongando o tempo de incubação dos anticorpos) para melhorar as taxas de deteção. | Valide o título de anticorpos em pré-experimentos; enriqueça para alvos altamente expressos. |
| Baixo ruído de fundo (FRiP > 10%) | Não é possível distinguir locais de ligação fisicamente adjacentes. | Integre dados de ATAC-seq ou Hi-C para resolver interações tridimensionais. |
| Ciclo experimental curto (concluído em 24 horas) | Alto custo para experiências de célula única | Adote plataformas como a 10x Genomics para reduzir o custo por amostra. |
VII. Protocolo Experimental Recomendada (Tomando o fator de transcrição CTCF como exemplo)
- Preparação de Amostras:
- Tipo de Célula: Linha celular de câncer colorretal HCT116 (viabilidade >90%).
- Volume Inicial: 5.000 células, lavadas com PBS e ressuspendidas em 1× PBS + 0,1% BSA.
- Incubação de Anticorpos:
- Anticorpo Primário: anticorpo CTCF (Abcam #ab150471), diluição 1:100, incubado durante a noite a 4°C.
- Anticorpo Secundário: Cabra anti-rato IgG (Jackson ImmunoResearch #111-005-003), diluição 1:200, incubado à temperatura ambiente durante 1 hora.
- Reação de Transposição: enzima pA-Tn5, ativada a 37°C durante 8 minutos, DNA purificado após a interrupção da reação.
- Construção de Biblioteca: Kit de Preparação de Biblioteca de DNA NEBNext Ultra II, amplificação por PCR 12 ciclos, tamanho do fragmento selecionado 200–400 bp.
- Sequenciação e Análise:
- Plataforma: Illumina NovaSeq 6000, PE150, 15M leituras/amostra.
- Fluxo de Análise: identificação de picos MACS2 → análise de motivos HOMER → anotação diferencial de picos.
VIII. Direções Futuras de Desenvolvimento Tecnológico
- Integração de multi-ómica de célula única: Combinando scCUT&Tag com scATAC-seq para elucidar a dinâmica espaciotemporal da acessibilidade da cromatina e da ligação de proteínas.
- Adaptação de sequenciação por nanopore: Desenvolvimento de esquemas de construção de bibliotecas CUT&Tag compatíveis com sequenciação de leituras longas para capturar elementos regulatórios complexos.
- Automação e assistência de IA: Otimização das taxas de sucesso experimental através da previsão das condições de incubação de anticorpos com base em aprendizagem automática.
As pessoas também perguntam
Como funciona a tagmentação Tn5?
A Illumina desenvolveu o protocolo de tagmentação, no qual uma enzima Tn5 modificada corta o DNA de cadeia dupla e, simultaneamente, liga as sequências de ligadura que são necessárias para o sequenciamento da Illumina a ambas as extremidades.
Qual é o mecanismo de inserção do Tn5?
O Tn5 consiste em duas sequências de inserção IS50 que envolvem três genes que codificam resistência à kanamicina, bleomicina e estreptomicina. A transposição do Tn5 ocorre através de um mecanismo de corte e colagem, movendo o transposão do doador para o alvo, sem criar cópias adicionais do transposão.
Qual é o processo de tagmentação?
A tagmentação é o passo inicial na preparação da biblioteca onde o DNA não fragmentado é clivado e etiquetado para análise. A preparação da biblioteca por tagmentação em beads utiliza transposomas ligados a beads para uma reação de tagmentação mais uniforme em comparação com reações de tagmentação em solução.
Como funciona a transposase Tn5 no Atac Seq?
O Tn5 fragmenta simultaneamente o DNA, insere-se preferencialmente em locais de cromatina aberta e adiciona primers de sequenciação (um processo conhecido como tagmentação). O DNA sequenciado identifica a cromatina aberta e a análise de dados pode fornecer informações sobre a regulação genética.
Qual é o viés da sequência da transposase Tn5?
O Tn5 apresenta um viés de sequência complexo que não é efetivamente ajustado com métodos tradicionais de correção de viés.
Referências:
- Abbasova L, Urbanaviciute P, Hu D, Ismail JN, Schilder BM, Nott A, Skene NG, Marzi SJ. CUT&Tag recupera até metade dos picos de acetilação de histonas do ENCODE ChIP-seq. Nat Commun. 2025 Mar 27;16(1):2993.
- Henikoff S, Henikoff JG, Ahmad K, Paranal RM, Janssens DH, Russell ZR, Szulzewsky F, Kugel S, Holland EC. Análise epigenómica de amostras fixadas em formalina e incorporadas em parafina por CUT&Tag. Nat Commun. 22 de setembro de 2023;14(1):5930.


 Diretrizes para Submissão de Amostras
Diretrizes para Submissão de Amostras
